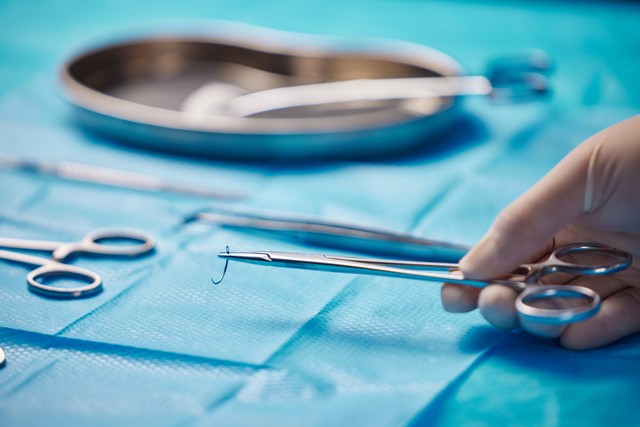
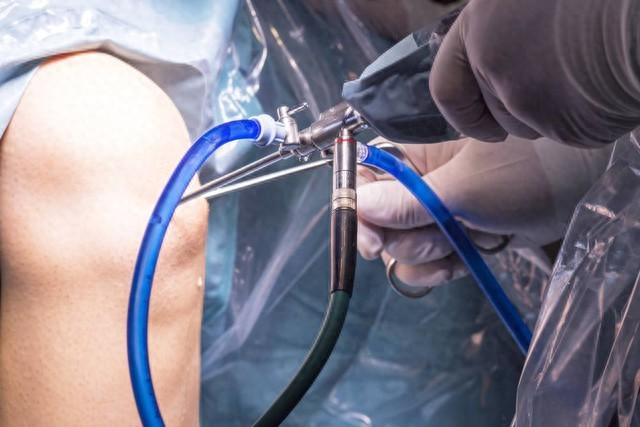
医疗器械唯一标识(UDI)追溯系统搭建流程
医疗器械唯一标识(UDI)追溯系统的搭建是一个涉及多个步骤的过程,主要包括以下几个环节:

1. 组建UDI团队
首先,企业需要组建一个专门的UDI团队,这个团队应包括负责法规注册的人员、负责IT信息相关的人员、研发人员、负责生产方面的人员、负责质量控制的人员、销售人员、负责把控供应链及物流的人员,以及进行营运管理的人员。这样做的目的是确保UDI实施过程中各个部门能够相互配合协作,共同解决问题。以上由慧铭佳UDI整理
2. 选择发码机构
接下来,企业需要选择一个经过国家药品监督管理局认证的发码机构。这样的机构通常有三家,分别是“中国物品编码中心(GS1)”,“中关村工信二维码技术研究院(MA)”和“阿里健康科技(中国)有限公司(AHM)”。价格和编码规则都会有所不同,企业需要根据自己的需求选择合适的机构。
3. 完成发码机构选择后的申报流程
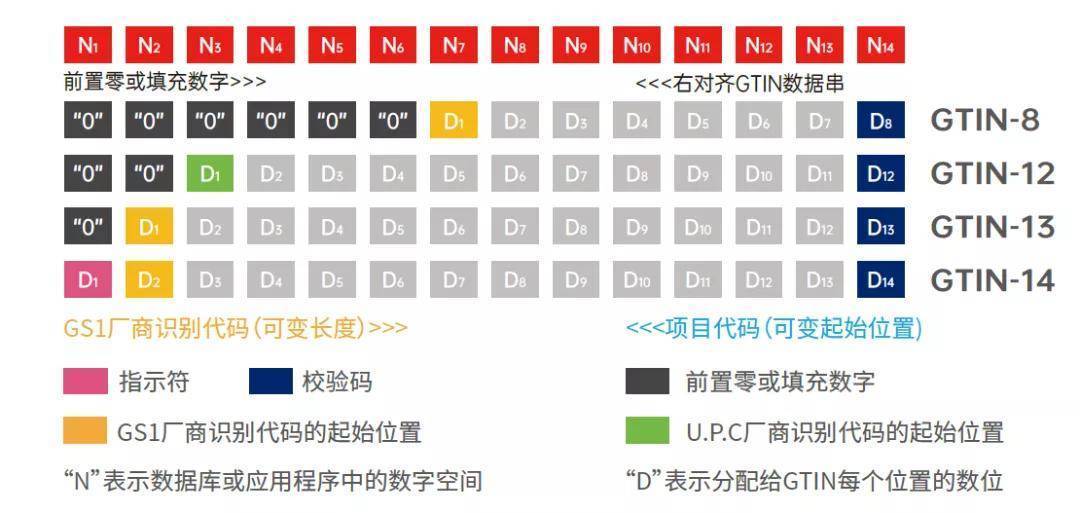
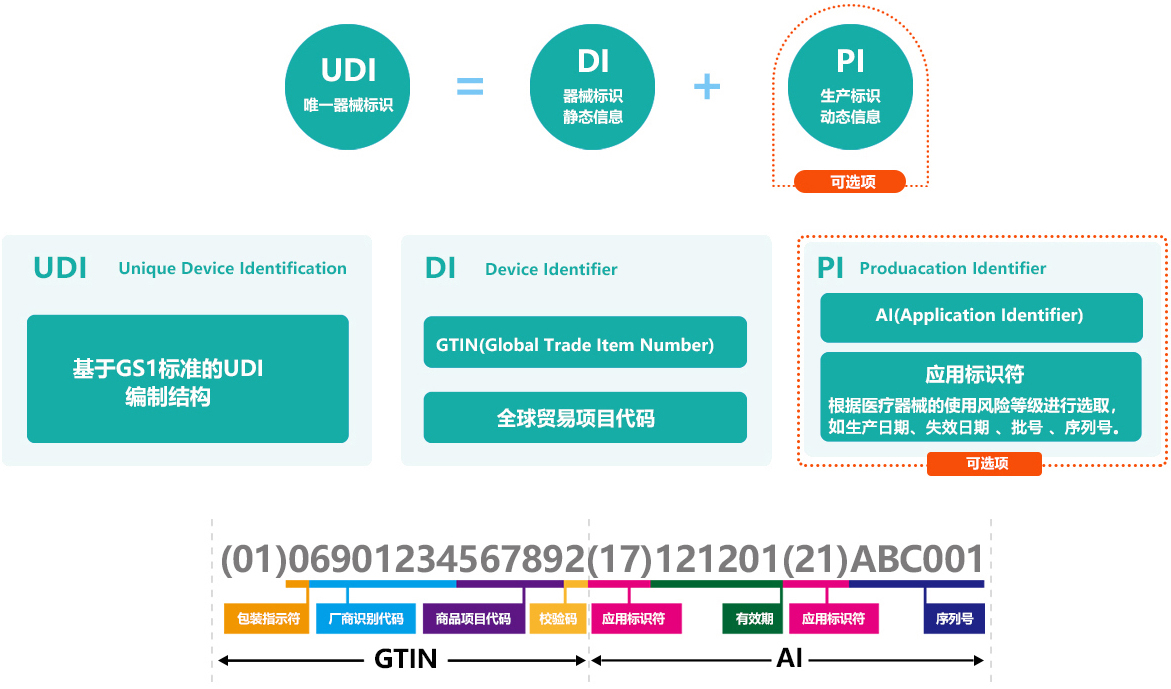
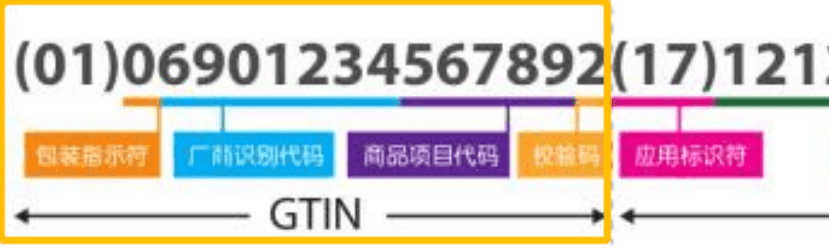
完成发码机构的选择后,企业需要按照该机构的不同流程进行注册缴费,并得到DI编码。然后,企业根据编码规则进行编码和校检,并登陆药监局平台填写产品信息,将DI编码上报至药监局平台。药监局数据库会对所有DI数据进行审核,并公布申报情况。以上由慧铭佳UDI整理
4. 设计和打印UDI标签
审核通过后,企业需要开始设计二维码标签,并确保标签的设计原则得到遵守,例如必须同时附带一维条码或二维码标签,标签不能仅有码图,需要同时附有中文标识说明,标签印刷质量需符合ISO15415标准的C级以上,UDI编码与码图扫码内容必须一致、正确等。
5. 建立UDI数据库
将医疗器械的UDI编码、生产商信息、产品信息等录入数据库,实现信息的共享和查询。
6. 应用UDI追溯系统
最后,企业需要将UDI追溯系统应用于医疗器械的生产、流通、使用等全过程,实现全流程的追溯和监管。同时,还需要定期维护UDI数据库,更新数据库信息,保证UDI信息的准确性和完整性。
注意事项
企业在搭建UDI追溯系统的过程中,需要注意保护数据的安全,确保数据的准确性和完整性。此外,还需要确保UDI标签的设计和印刷质量,以满足自动识别和数据采集技术以及人工识读的要求。同时,企业应积极参与相关的培训和指导,以便更好地理解和掌握UDI追溯系统的搭建流程和技术要点。
 UDI网-UDI申请编码赋码软件专业知识网
UDI网-UDI申请编码赋码软件专业知识网