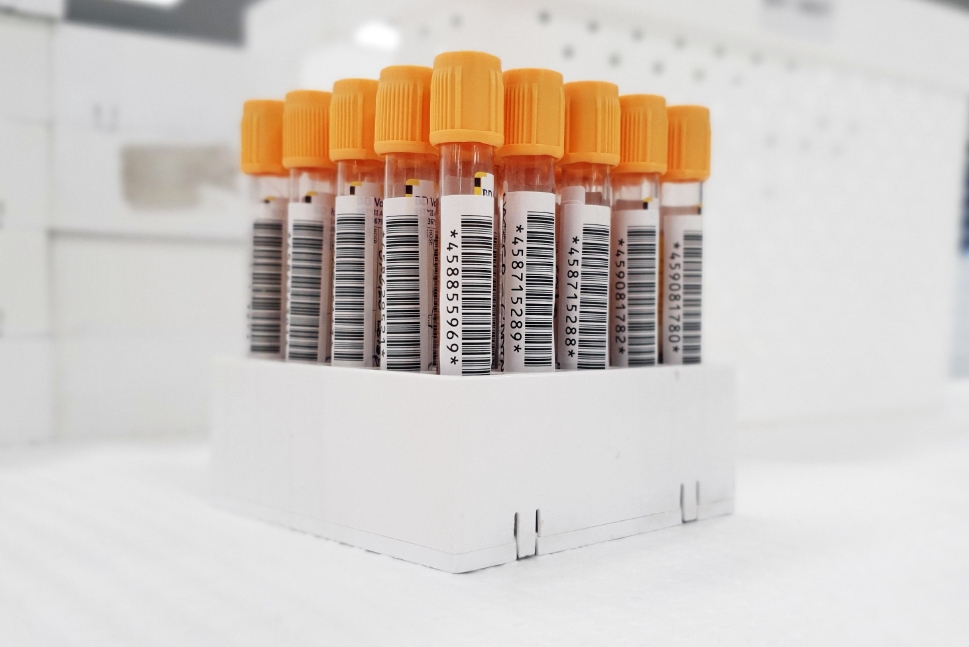
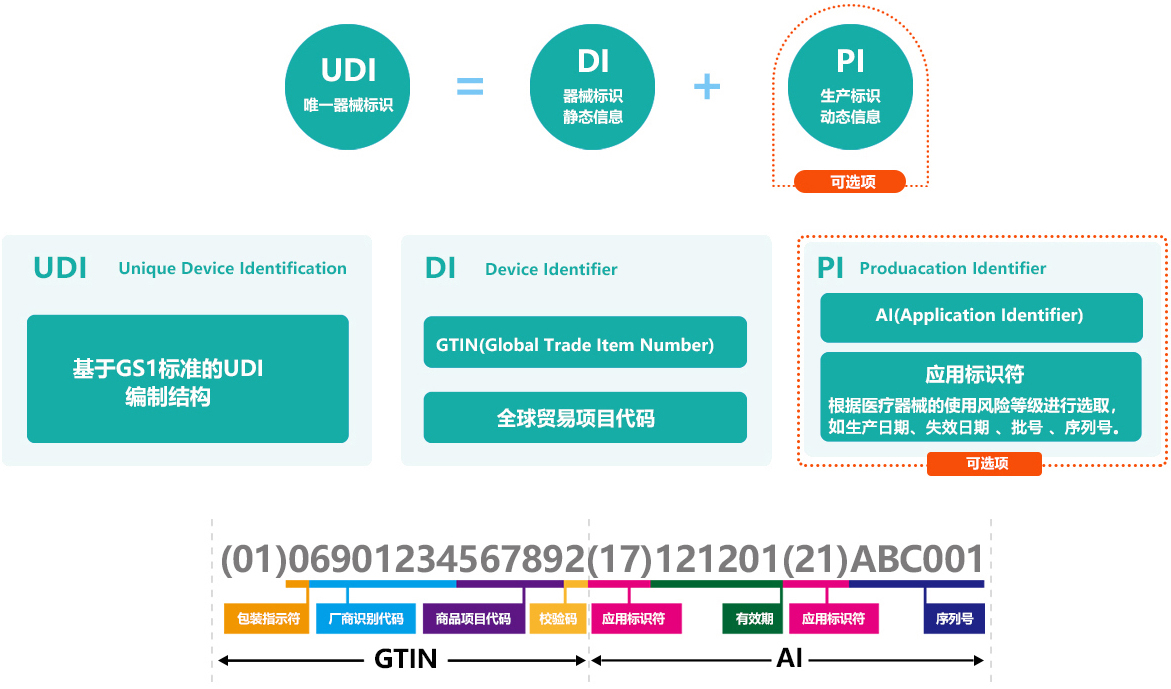
中国UDI的“基本法”是《医疗器械唯一标识系统规则》,这个规则是2019年8月发布的。其基本目的是为了贯彻落实《国务院办公厅关于印发治理高值医用耗材改革方案的通知》(国办发〔2019〕37号),规范医疗器械唯一标识系统建设,加强医疗器械全生命周期管理。
首先回顾一下中国医疗器械UDI实施的一些关键时间点:
2019年7月——【药监综械注〔2019〕56号】 关于印发医疗器械唯一标识系统试点工作方案的通知:拉开了中国UDI的序幕;
2019年8月——【2019年第66号】国家药监局关于发布医疗器械唯一标识系统规则的公告:中国UDI的规则被正式建立;
2019年10月——【2019年第72号】国家药监局关于做好第一批实施医疗器械唯一标识工作有关事项的通告:明确了第一批实施产品及其时间点;
2019年12月——UDI数据库正式上线;
2020年9月——【2020年第106号】关于深入推进试点做好第一批实施医疗器械唯一标识工作的公告:第一批实施产品时间点推迟到2021年1月1日。
第一批:2019年10月,国家药监局发布《国家药监局关于做好第一批实施医疗器械唯一标识工作有关事项的通告》,要求按照风险程度和监管需要,确定部分有源植入类、无源植入类等高风险第三类医疗器械作为第一批医疗器械唯一标识实施品种。
第一批补充:由于疫情原因,在2020年9月,国家药监局发布《国家药监局 国家卫生健康委 国家医保局关于深入推进试点做好第一批实施医疗器械唯一标识工作的公告(2020年 第106号)》,要求在《国家药监局关于做好第一批实施医疗器械唯一标识工作有关事项的通告》(2019年第72号)9大类64个品种的基础上,将《清单》中耳内假体、脊柱椎体间固定/置换系统、可吸收外科止血材料、阴茎假体、植入式药物输注设备等5种高风险第三类医疗器械纳入第一批实施唯一标识的品种范围。
第二批:2021年9月,国家药监局发布《国家药监局 国家卫生健康委 国家医保局关于做好第二批实施医疗器械唯一标识工作的公告(2021年第114号 )》,要求在《国家药监局 国家卫生健康委 国家医保局关于深入推进试点做好第一批实施医疗器械唯一标识工作的公告》(2020年 第106号)规定的9大类69个品种的基础上,将其余第三类医疗器械(含体外诊断试剂)纳入第二批实施唯一标识范围。
第三批:2023年2月,国家药监局发布《国家药监局 国家卫生健康委 国家医保局关于做好第三批实施医疗器械唯一标识工作的公告(2023年第22号)》,在第一批和第二批实施的基础上,按照风险程度和监管需要,确定部分临床需求量较大的一次性使用产品、列入医保集采范围的品种、医疗美容相关产品等部分第二类医疗器械,共141个品种,作为第三批医疗器械唯一标识实施品种。
第一批实施UDI器械
政策文件:《关于做好第一批实施医疗器械唯一标识工作有关事项的通告》(2019年第72号)
实施时间:2021年1月1日
实施品种:部分有源植入类、无源植入类等高风险第三类医疗器械。
第二批实施UDI器械
政策文件:《关于做好第二批实施医疗器械唯一标识工作的公告》(2021年第114号)
实施时间:2022年6月1日
实施品种:在第一批9大类69个品种的基础上,将其余第三类医疗器械(含体外诊断试剂)纳入第二批实施唯一标识范围。
第三批实施UDI器械
政策文件:《关于做好第三批实施医疗器械唯一标识工作的公告》(2023年第22号)
实施时间:2024年6月1日
实施品种:部分临床需求量较大的一次性使用产品、集中带量采购中选产品、医疗美容相关产品等部分第二类医疗器械
 UDI网-UDI申请编码赋码软件专业知识网
UDI网-UDI申请编码赋码软件专业知识网