概述:
本文主要介绍了2024年最新版中国、美国和欧盟在医疗器械查询政策方面的50条网站总汇。这些网站涵盖了各种医疗器械的相关信息,包括产品注册、认证、监管等方面的内容。这对于医疗器械行业的企业和从业人员来说,是一个非常有价值的资源。通过查阅这些网站,可以了解到最新的医疗器械政策动态和市场趋势,从而更好地把握行业发展方向。
中、美、欧医疗器械相关信息网址
中国
1. 国家药品监督管理局 (NMPA)
www.nmpa.gov.cn
介绍: 中国的官方药品和医疗器械监管机构的主页,提供政策法规、公告通知、药品和医疗器械的审批信息等。
2. 国家药品监督管理局 数据查询
http://app1.nmpa.gov.cn/data_nmpa/face3/dir.html?CbSlDlH0=qGcbkAr_8vN_8vN_8jp1szy7ruD4OwTMgq0JwJJKdoQqqoL
介绍:该页面提供药品和医疗器械的注册信息、生产信息、批准文号等数据的查询服务。
3. 医疗器械标准查询
http://app.nifdc.org.cn/biaogzx/qxqwk.do
介绍: 用户可以通过此平台查询医疗器械的国家标准和行业标准。
4. 医疗器械行业标准
http://app.nifdc.org.cn/jianybz/jybzTwoGj.do?formAction=listTsDalid&type=ylqx&page=list_ylqx
介绍: 提供医疗器械行业标准的列表和详细信息。
5. 医疗器械非采标推荐性行业标准
http://app.nifdc.org.cn/jianybz/jybzTwoGj.do?formAction=listTsDalid&type=qxtjbz&page=list_qxtjbz
介绍: 非强制性推荐的医疗器械行业标准,供企业参考使用。
6. 医疗器械分类目录查询
http://app.nifdc.org.cn/biaogzx/dataGk.do
介绍: 用户可以查询医疗器械的分类目录,了解不同产品的分类信息。
7. 分类界定文件查询
http://app.nifdc.org.cn/biaogzx/flmlbczlk.do
介绍: 提供医疗器械分类界定的文件查询服务。
8. I类产品补充分类信息
http://app.nifdc.org.cn/biaogzx/flmlbczlk.do
介绍: 针对I类医疗器械产品的补充分类信息查询。
9. 医疗器械标准与分类管理
https://www.nifdc.org.cn/nifdc/bshff/ylqxbzhgl/index.html
介绍: 介绍医疗器械的标准和分类管理体系。
10. 医疗器械法规查询
https://www.nmpa.gov.cn/xxgk/fgwj/index.html
介绍: 提供医疗器械相关的法规查询服务。
11. 国家标准全文公开系统
http://openstd.samr.gov.cn/bzgk/gb/index
介绍: 公开国家标准的全文,包括医疗器械相关标准。
12. 分类目录指导原则标准
https://www.cmde.org.cn/CL0195/
介绍: 提供医疗器械分类目录、指导原则和标准的查询。
13. 审评论坛
https://www.cmde.org.cn/CL0010/
介绍: 医疗器械审评相关的论坛,供业内人士交流。
14. 医疗器械交流论坛
https://pd.qq.com/s/9lgtmt5wz
介绍: 一个医疗器械行业的交流论坛。
15. 国家局器审中心
https://www.cmde.org.cn/CL0001/
介绍: 国家药品监督管理局的医疗器械审评中心。
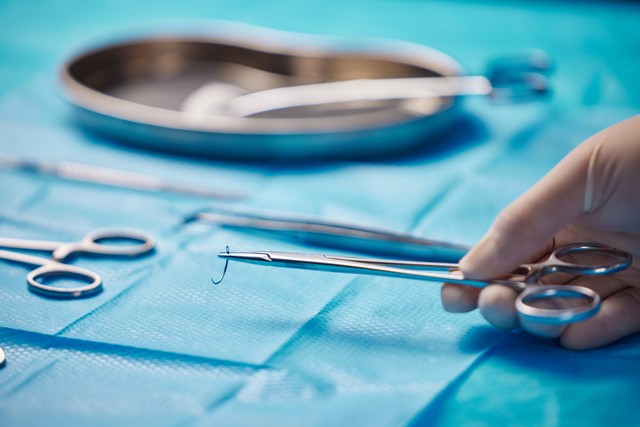
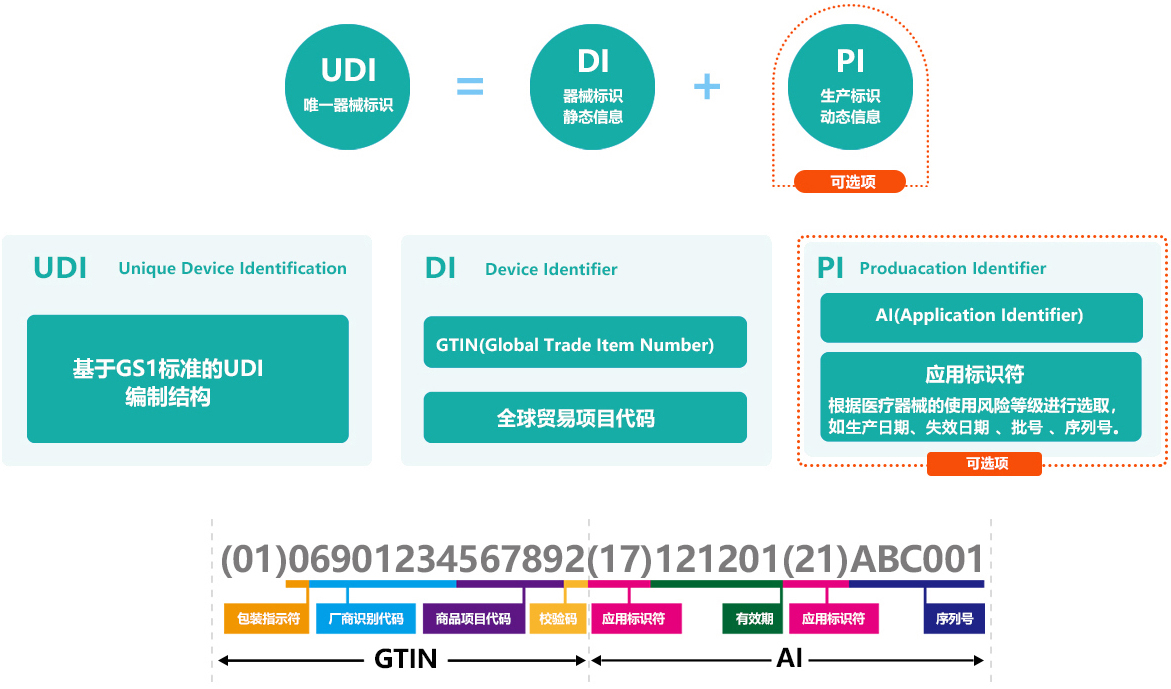
16. 医疗器械UDI数据库
https://udi.nmpa.gov.cn/
介绍: 医疗器械的唯一标识(UDI)数据库。
17. 医疗器械不良事件通报
https://www.nmpa.gov.cn/xxgk/yjjsh/ylqxblshjtb/index.html
介绍: 发布医疗器械不良事件的通报。
18. 医疗器械召回
https://www.nmpa.gov.cn/xxgk/chpzhh/ylqxzhh/index.html
介绍: 发布医疗器械召回的通知。
19. 国家局高级研修学院
http://nmpaied.org.cn/
介绍: 国家药品监督管理局的高级研修学院。
20. 国家医疗器械不良事件监测信息系统
https://maers.adrs.org.cn/console/login.ftl
介绍:国家医疗器械不良事件监测的信息系统
21. 第三方医疗器械法规合集
https://www.jcyyzx.com/4/6.html
介绍:这个网站收集了与医疗器械相关的各种法规和指南,由第三方提供,便于业内人士参考和查阅。
22. 国家局审核查验中心
https://www.cfdi.org.cn/cfdi/index?module=A001&nty=A25
介绍:国家药品监督管理局的审核查验中心,负责对医疗器械等进行审核和检查。
23. 国家药品监督管理局医疗器械技术审评中心
https://www.cmde.org.cn/CL0279/
介绍: 国家药品监督管理局医疗器械技术审评中心专门负责审核医疗器械的安全和有效性。
欧盟
1. 欧盟医疗器械信息
https://ec.europa.eu/health/md_sector/overview_en
介绍: 欧盟医疗器械部门提供的概览页面,包括行业新闻、立法动态和相关信息。
2. 欧盟医疗器械专家委员会
https://ec.europa.eu/health/md_expertpanels/overview_en
介绍: 欧盟医疗器械专家委员会负责提供专业意见和指导,以确保医疗器械的安全性和有效性。
3. EUDAMED
https://ec.europa.eu/health/md_eudamed/overview_en
介绍: EUDAMED是欧盟建立的医疗器械数据库,提供注册、认证和监管信息,以促进欧盟医疗器械监管体系的透明度和互操作性。
4. EUDAMED数据库
https://webgate.ec.europa.eu/eudamed/landing-page#/
介绍: 访问EUDAMED数据库,查询医疗器械相关的注册、认证和监管信息。
5. 医疗器械协调小组工作组
https://ec.europa.eu/health/md_dialogue/mdcg_working_groups_en
介绍: 医疗器械协调小组(MDCG)的工作组负责制定和更新指导文件,以协助欧盟成员国实施医疗器械法规。
6. MDCG指南
https://ec.europa.eu/health/md_sector/new_regulations/guidance_en#sec
介绍: MDCG提供的医疗器械法规指南,帮助制造商和监管机构理解和遵守法规要求。
7. 欧盟协调标准
https://ec.europa.eu/growth/single-market/european-standards/harmonised-standards_en
介绍: 欧盟协调标准是欧洲标准的一部分,为医疗器械提供安全和性能要求的标准。
8. Basic UDI-DI生成
https://www.gs1.org/services/gmn-generator
介绍: GS1提供的工具,用于生成基本的全球唯一设备标识符(UDI-DI)。
9. 公告机构Nando EUROPA - 欧洲委员会 - 增长 - 监管政策 - NANDO
https://ec.europa.eu/growth/toolsdatabases/nando/index.cfm?fuseaction=notifiedbody.main
介绍: NANDO数据库提供欧盟认可的公告机构信息,这些机构负责对医疗器械进行认证和监管。
10. NB-MED文件
https://www.team-nb.org/nb-med-documents/
介绍: NB-MED是欧洲合格评定机构网络(TEAM-NB)提供的文件,涉及医疗器械的认证和监管。
美国
1. 美国FDA
https://www.fda.gov/
介绍: 美国FDA是负责监管美国市场食品、药品和医疗器械的联邦机构。
2. 美国联邦法规
https://www.ecfr.gov/cgi-bin/text-idx?SID=3ee286332416f26a91d9e6d786a604ab&mc=true&tpl=/ecfrbrowse/Title21/21tab_02.tpl
介绍: 提供美国联邦法规的在线浏览,包括FDA相关的法规。
3. 医疗器械数据库
https://www.fda.gov/medical-devices/device-advice-comprehensive-regulatory-assistance/medical-device-databases
介绍: 提供医疗器械的综合监管援助信息,包括数据库查询。
4. CDRH Learn
https://www.fda.gov/training-and-continuing-education/cdrh-learn
介绍: FDA下属的设备中心(CDRH)提供的在线培训和教育资源。
5. 510(k) premarket notification
https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfPMN/pmn.cfm
介绍: 510(k)是FDA规定的一种医疗器械上市前通知程序。
6. 工厂注册和器械列名
https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfRL/rl.cfm
介绍: 工厂注册和器械列名的FDA程序和要求。
7. 产品分类数据库
https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfpcd/classification.cfm
介绍: 提供FDA对医疗器械产品的分类信息。
8. FDA认可标准数据库
https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfStandards/search.cfm
介绍: 查询FDA认可的医疗器械相关标准。
9. 审评指南数据库
https://www.fda.gov/medical-devices/device-advice-comprehensive-regulatory-assistance/guidance-documents-medical-devices-and-radiation-emitting-products
介绍: 提供FDA医疗器械审评的指南和文件。
10. FDA账号注册与登录
https://www.access.fda.gov/oaa/logonFlow.htm?execution=e1s1
介绍: 注册和登录FDA的账号,以访问特定的FDA系统和服务。
11. FDA自由信息法案
https://www.fda.gov/regulatory-information/freedom-information
介绍: 关于FDA如何处理自由信息法案请求的信息。
12. FDA法规简介
https://www.fda.gov/medical-devices/device-advice-comprehensive-regulatory-assistance
介绍: 提供FDA医疗器械法规的概览和指导。
13. FDA UDI
https://www.fda.gov/medical-devices/device-advice-comprehensive-regulatory-assistance/unique-device-identification-system-udi-system#ruleguidance
介绍: 介绍FDA的唯一设备标识(UDI)系统。
14. FDA MDSAP
https://www.fda.gov/medical-devices/cdrh-international-programs/medical-device-single-audit-program-mdsap
介绍: 介绍FDA的医疗器械单一审核程序(MDSAP)。
15. MDR上报
https://www.fda.gov/medical-devices/medical-device-safety/reporting-allegations-regulatory-misconduct
介绍: 如何向FDA报告医疗器械相关的安全问题。
16. 召回数据库
https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfRES/res.cfm
介绍: 查询FDA医疗器械召回数据库。
17. GUDID数据库
https://accessgudid.nlm.nih.gov/
介绍: GUDID是FDA建立的全球唯一设备标识(UDI)数据库的一部分,它提供了UDI的数据元和标签规范,以及与UDI相关的设备识别信息。
18. OSHA的全国公认测试实验室(NRTL)
https://www.osha.gov/nationally-recognized-testing-laboratory-program
介绍: OSHA的NRTL计划认可的第三方测试实验室,这些实验室对设备和产品进行测试以确保它们符合OSHA的安全标准。这些实验室对医疗器械的安全性和合规性进行评估。
 UDI网-UDI申请编码赋码软件专业知识网
UDI网-UDI申请编码赋码软件专业知识网