有源植入器械
01 心脏节律管理设备
10 起搏系统分析设备 II
描述:通常由分析仪主机和患者电缆、电缆适配器、无菌延长线组成。
预期用途:适合在起搏器和除颤器植入过程中用于对起搏电极系统进行分析。以上由慧铭佳UDI整理
举例:起搏系统分析仪
管理类别:II

11 心脏节律管理程控设备 II
描述:通常由显示单元、打印单元、程控单元、软件等组成。
预期用途:用于询问、程控、显示数据或测试植入式心脏起搏器和植入式心律转复除颤器等心脏节律管理设备。以上由慧铭佳UDI整理
举例:心脏节律管理设备程控仪、心脏节律管理设备患者程控仪、程控仪
管理类别:II
12 连接器套筒 II
描述:通常由接触夹及连接器环形电极组成。
预期用途:用于连接到电极导线连接器、或者断开连接。
举例:四极连接器套筒,以上由慧铭佳UDI整理
管理类别:II
02 神经调控设备
07 测试刺激器 II
描述:通常由控制单元、输出单元、电源单元组成。
预期用途:用于在电极导线放置或试验刺激效果期间评估神经刺激系统的功效。以上由慧铭佳UDI整理
举例:测试神经刺激器、测试刺激器、体外神经刺激器
管理类别:II
08 测试延伸导线 II
描述:通常由延伸导线和附件(若使用)组成。
预期用途:与测试刺激器、配合使用,用于临时刺激和测试。
举例:测试神经刺激延伸导线、神经刺激系统经皮延伸导线和电缆、多电极测试电缆,以上由慧铭佳UDI整理
管理类别:II
09 神经调控程控设备 II
描述:通常由程控单元、显示单元、软件等组成。
预期用途:用于对植入式神经调控设备的询问、程控、显示数据和测试。
举例:神经调控设备程控仪、神经调控设备患者程控仪、程控仪、患者程控仪,以上由慧铭佳UDI整理
管理类别:II
03 辅助位听觉设备
02 体外声音处理器 II
描述:通常由言语处理器主机、控制器等组成的体外部分。
预期用途:与植入式辅助听觉设备体配合使用,将声音转化为电刺激或振动,通过对耳蜗内或蜗后听觉传导通路特定部位进行电刺激,或对中耳以及骨传导进行振,以上由慧铭佳UDI整理
动来提高或恢复听觉感知。
举例:人工耳蜗声音处理器、振动声桥系声音处理器、骨桥声音处理器、骨导声音处理器
管理类别:II
03 辅助位听觉调控设备 II
描述:通常由主机,连接电缆等组成。
预期用途:用于调试或测试辅助位听觉设备。
举例:人工耳蜗调机设备、振动声桥调机设备、骨桥调机设备、人工耳蜗检测设备
管理类别:II
04 其他
01 植入式心脏收缩力调节设备
描述:通常由显示单元、程控单元、软件等组成。
预期用途:用于询问、程控、显示数据或测试植入式心脏收缩力调节设备。
举例:心脏收缩力调节设备程控仪
管理类别:II类部分
有源植入器械UDI的实施情况
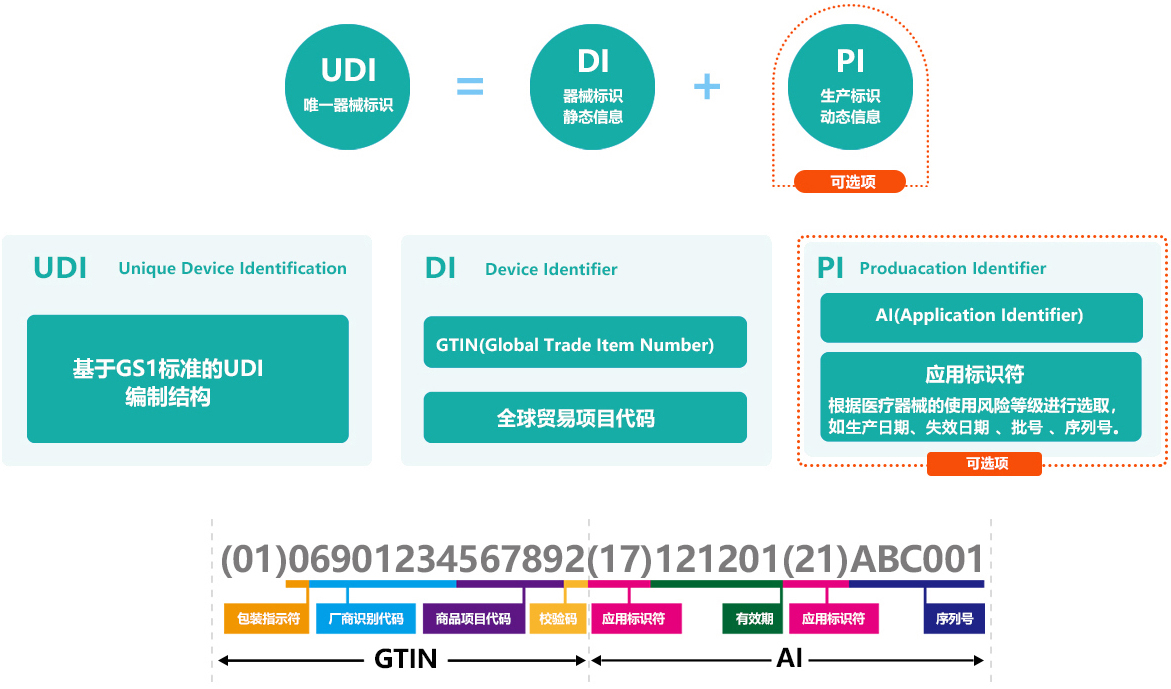
根据搜索结果,有源植入器械是第一批实施UDI的高风险第三类医疗器械之一。具体来说,对于有源植入器械,其UDI-PI应至少包括序列号;对于其他可植入器械,则为序列号或批号。此外,有源植入器械目录中包含了多种具体的有源植入器械,如植入式心脏起搏器、植入式心律转复除颤器等。
有源植入器械UDI的实施时间和范围
根据相关规定,自2021年1月1日起,有源植入类、无源植入类等高风险第三类医疗器械被确定为第一批医疗器械唯一标识实施品种。这批品种涵盖了9大类产品,包括有源手术器械、无源手术器械、神经和心血管手术器械等。
有源植入器械UDI的具体要求
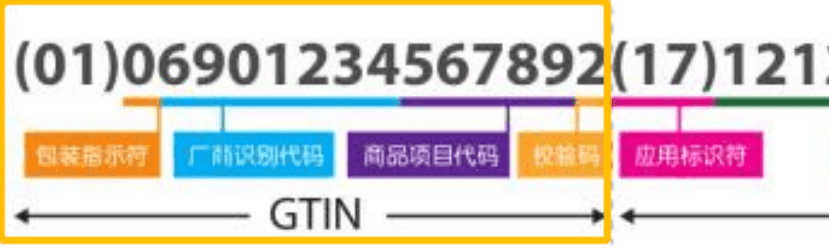
UDFI必须以纯文本版本/人类可读信息(HRI)以及使用AIDC技术的形式出现。AIDC指以可通过自动化过程输入电子病历或其他计算机系统的形式传达唯一器械标识符或器械的器械标识符的任何技术。HRI由易于阅读的清晰字符组成。对于专门用于零售点的器械,不需要AIDC中的UDI-PI出现在销售点包装上。
有源植入器械UDI的实施意义
UDI的实施可以帮助医疗器械注册人备案人更快建立追溯体系,在医疗器械全生命周期监管中准确识别产品,以进一步规范医疗器械的生产销售和临床使用。随着第二批UDI的实施,有码医疗器械产品数量会相应增多,有望进一步提高经营企业管理质效。
 UDI网-UDI申请编码赋码软件专业知识网
UDI网-UDI申请编码赋码软件专业知识网