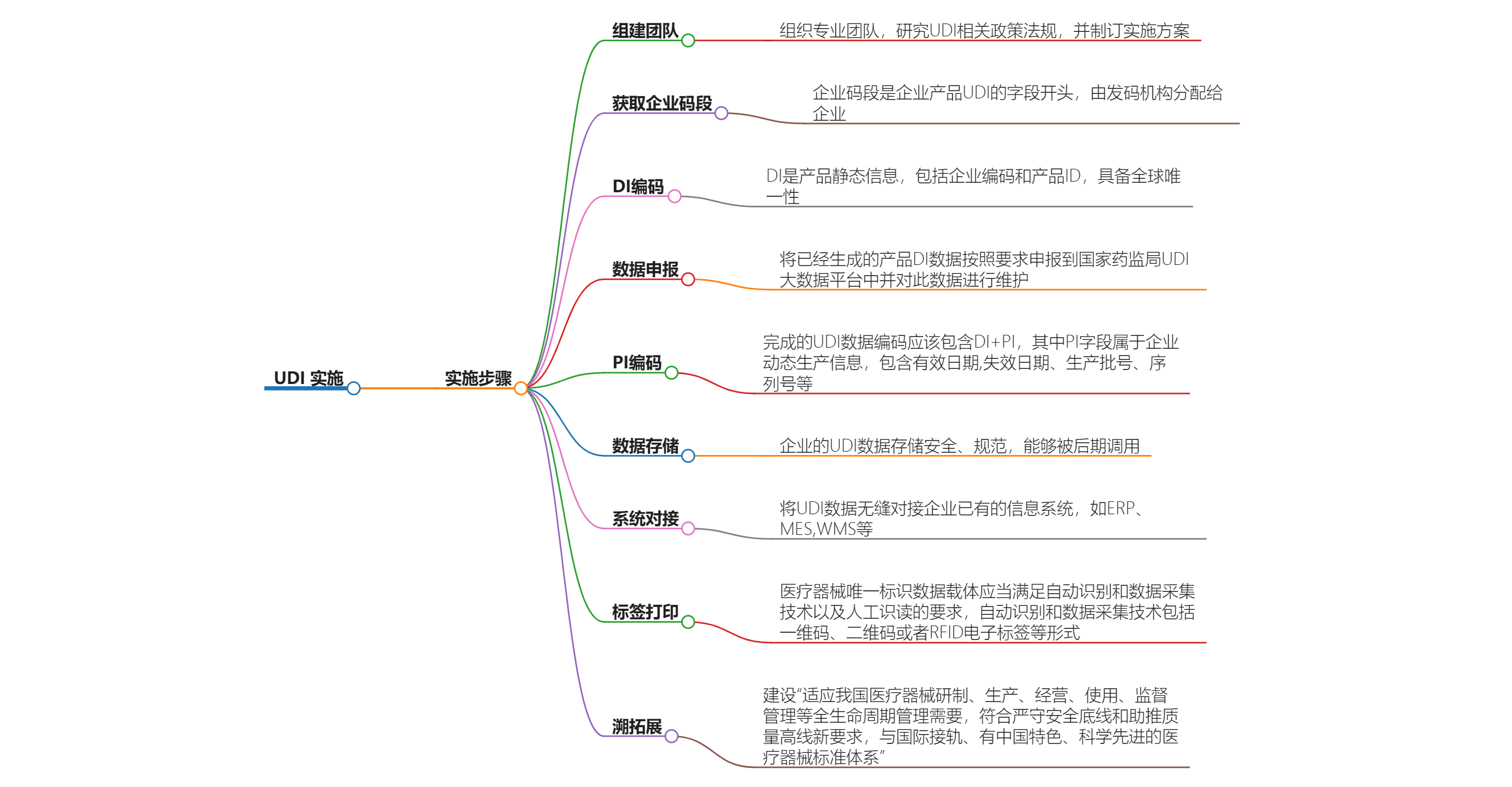
UDI 实施步骤概述
医疗器械唯一标识(UDI)的实施是一个系统的过程,主要包括以下几个步骤:
1. 组建UDI实施团队 and 制定实施方案
首先,企业需要组建专业的UDI实施团队,这个团队需要提前研究UDI的相关政策法规,并制定出详细的实施方案。如果是通过UDI公共平台进行实施,则只需要安排专人对接即可。
2. 获取企业码段
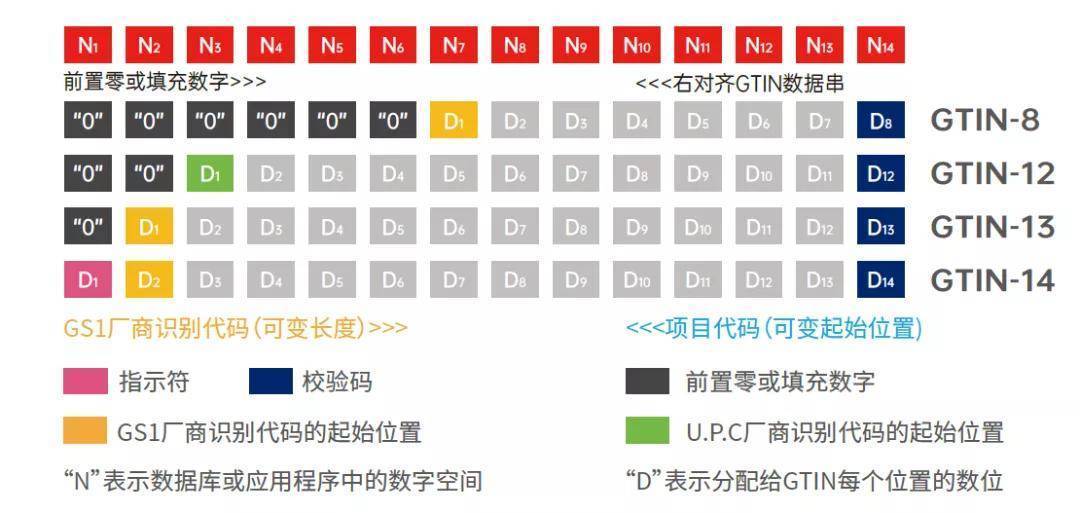
企业码段是企业产品UDI的字段开头,它唯一代表企业,由发码机构分配给企业。企业不可自己编辑,机构给到企业分配的企业码段是企业UDI数据识别和解析的重要组成部分,不可缺少。
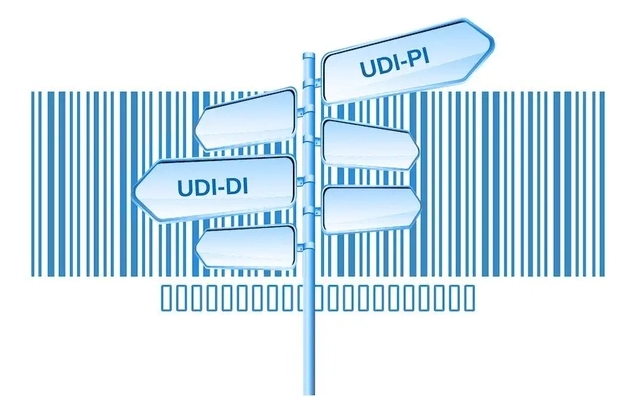
3. UDI编码
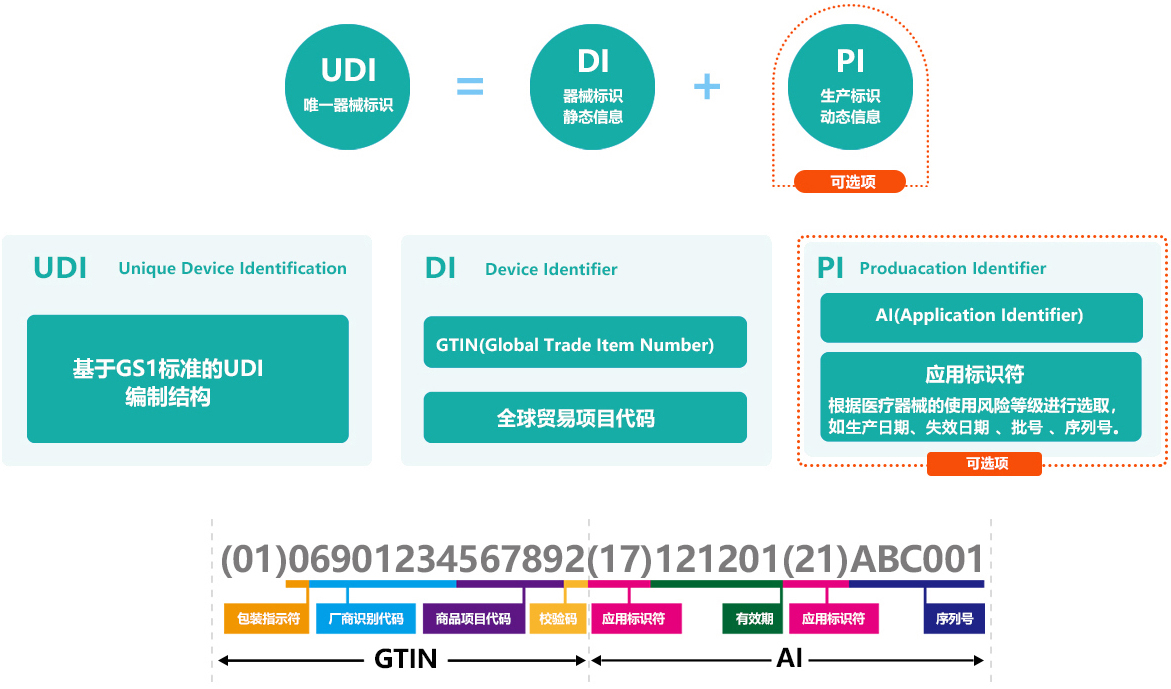
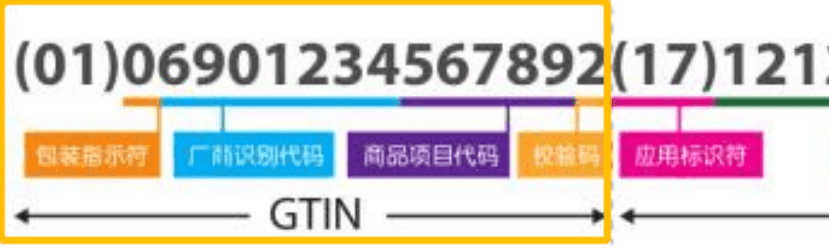
UDI编码是由产品标识(DI)和生产标识(PI)组成,产品标识(DI)是识别注册人/备案人、医疗器械型号规格和包装的唯一代码,是从数据库获取医疗器械相关信息的“关键字”,是唯一标识的必需部分;生产标识(PI)包括与生产过程相关的信息,比如产品批号、序列号、生产日期和失效日期等。
4. 数据申报
数据申报是指企业需要把已经生成的产品DI数据按照要求申报到国家药监局UDI大数据平台中并对此数据进行维护。在此之前,企业需要先完成国家药监局网上办事大厅企业账号开通和医疗器械唯一标识数据库企业账号的申请等一系列准备工作。
5. UDI赋码
UDI赋码是将UDI编码应用到医疗器械上的过程,通常通过喷码设备对产品进行赋码,为其赋予唯一身份标识。
6. UDI产品追溯
利用UDI码进行追溯管理,有利于不良事件的监控和问题产品召回,提高医疗质量,保障患者安全。每一台工控平台会生成不同的UDI码,所有产品UDI码都是现场生成,由现场工控平台上传至UDI追溯后台。
7. UDI应用拓展
基于UDI开放追溯、防伪、防窜等延伸应用,例如,实现扫码入库及出库,记录产品流向,或者在经营活动中积极应用唯一标识,做好带码入库、出库,实现产品在流通环节可追溯。
以上就是UDI实施的基本步骤,具体的操作可能会因为企业和地区的不同而有所差异。在实施过程中,可能还需要考虑到一些额外的因素,比如企业的信息化水平、法律法规的要求等。
 UDI网-UDI申请编码赋码软件专业知识网
UDI网-UDI申请编码赋码软件专业知识网